Валидация однородности смеси
Введение
Одна из серьезных проблем, с которыми на сегодняшний день сталкиваются производители твердых лекарственных форм, - это валидация однородности смеси. Несмотря на то, что речь идет только о единичной операции (процедуре), которая входит в состав общего процесса производства таблеток или капсул, для данной проблематики характерны определенные специфические аспекты, которые следует рассматривать самостоятельно.
Ряд современных сведений и требований, которые появляются при валидации таблеток или капсул, прямо или косвенно исходят из решения судьи Уолина в судебном процессе США против Barr Laboratories, который был связан с неудовлетворительным производством таблеток. Заключения, высказанные на этом процессе, много лет влияли на оценку производства твердых лекарственных форм, поэтому представляется необходимым включить их в валидационные исследования.
В настоящее время существуют два различных подхода к проведению валидации однородности смеси:
· подход FDA (исходящий из решения судьи Уолина)
· подход PDA (исходящий из статистического доказательства однородности)
Ниже по тексту будут приведены основные требования обоих подходов валидации смешения в различном оборудовании, таком как: смеситель-гранулятор, сушка в псевдоожиженом слое, V-образный смеситель. Для валидации однородности смеси будет подробно рассмотрен процесс PDA (Parenteral Drug Association).
Подход FDA
Именно решение судьи Уолина привело к тому, что FDA пересмотрела и модифицировала свою тактику по доказательству однородности смеси и методы пробоотбора. В результате возник подход, который исходит из предпосылки, что современная технология позволяет отобрать репрезентативные образцы из рабочих смесей. FDA требует, чтобы финишная смесь каждой серии проходила рутинное тестирование на однородность API (активного фармацевтического ингредиента), несмотря на адекватную валидацию процесса и другие проверки.
Применение решения судьи Уолина привело к введению следующих требований FDA по валидации однородности смеси:
1. образцы
• следует отбирать так, чтобы они были для данной смеси репрезентативными
· можно отбирать либо из смесителя (гомогенизатора), либо из контейнеров
· из всего объема смеси следует отобрать не меньше 10 образцов, в том числе и из возможных "мертвых зон"
· масса отдельного образца должна приближаться к трехкратной единичной дозе лекарственной формы
· можно отобрать и более крупные образцы, которые затем в лаборатории подлежат делению, но только в случае, если при обращении с ними предотвращено их дальнейшее смешивание или разделение (ослабление)
2. критерии приемлемости
· содержание API в каждом образце смеси должно соответствовать спецификации 90-110 % от заявленного значения
· максимальное относительное стандартное отклонение (RSD) для образцов смеси должно составлять 4 - 5 %
· РDА не рекомендует использовать при оценке
· однородности смеси лимиты для однородности содержания готовой продукции (85-115 %)
· более строгие критерии приемлемости необходимы, так как последующее хранение или переработка смеси на готовые таблетки либо капсулы может привести к разделению смеси
· слишком свободные критерии приемлемости (широкий диапазон) могут привести к выдаче разрешения на переработку смеси без обнаружения ошибок, а в результате - к ошибкам в содержании API в готовой продукции Q инспекция
· широкие критерии приемлемости (т.е. больше, чем 90 - 110%) для образца смеси считаются отклонением от современной надлежащей производственной практики - GMP
· отклонение менее значимо, если результаты по смеси находятся в пределах определения содержания в готовой продукции
· дефекты в однородности смеси для лекарственных средств с высокими дозами и широким терапевтическим диапазоном считаются менее значимыми, чем для лекарственных средств с низкой дозировкой и узким терапевтическим диапазоном действия
Подход PDA
В специальной литературе было опубликовано, что современная технология пробоотбора сталкивается с рядом проблем, и в сочетании с критериями приемлемости, которые не опираются на статистические методы, может привести к значимым ошибкам при валидации либо при тестировании смесей.
Поэтому комиссия по валидации процесса твердых лекарственных форм при PDA пересмотрела свой подход к анализу однородности смесей и выпустила техническую записку (Technical Report No. 25, 31end Uniformity Analysis: Validation and In-Process Testing"), чтобы объяснить аспекты, которые влияют на процессы валидации и критерии приемлемости. В названной технической записке описаны:
· метод определения соответствующего размера пробы Q голистический подход для валидации и критериев приемлемости
· использование правильных аналитических методов Q рекомендации по расследованию результатов OOS (вне рамок спецификации)
Вся техническая записка по проведению валидации однородности смеси опирается на размышления о смешивании и методы пробоотбора. Предполагается, что если процесс прошел один раз валидацикх то мониторинг его соответствия может проводиться путем тестирования готовой продукции. Рутинный анализ однородности смеси не обязательно проводить как тест производственного контроля в процессе, который был правильно специфицирован, правильно управляется и прошел валидацию.
Надежность валидации процесса зависит от комплексности подхода ко всем аспектам, которые влияют на смешивание. К ним относятся:
· спецификация ингредиентов и процессы QC
· квалификация и сертификация поставщика
· квалификация, техническое обслуживание и калибровка оборудования
· утвержденные и документированные процессы смешивания и грануляции (очередность, оборудование, время, скорость, и т.п.)
· контроль факторов окружающей среды, которые могут повлиять на смешивание (например, статический заряд, разложение активного ингредиента)
· контроль за изменениями
· обучение персонала
Валидация однородности смешивания
Из приведенной выше информации вытекает, что валидация однородности смеси - комплексная проблема. С практической позиции поэтому рекомендуется разделить все операции, связанные с доказательством однородности смеси и с проверкой процедуры смешивания, следующим образом:
Фаза до валидации (фаза оптимизации):
• пробоотбор порошковых смесей
• число образцов
• оптимизация параметров процесса фаза валидации (PDA)
• голистический подход
• анализ рассеяния/синтезом
Пробоотбор порошковых смесей
Пробоотборная игла либо полый пробоотборник представляют собой современное состояние технологии отбора проб. Доказательство однородности содержания смеси сложно как раз в связи с возможностью ошибки при пробоотборе (т.е., физико-химические свойства образца значимо отличаются от смеси, из которой он был отобран). Современная технология не предоставляет метода для универсального отбора малых репрезентативных образцов из крупных порошковых смесей.
На ошибку пробоотбора может влиять:
· исполнение пробоотборника
· методика пробоотбора
· физико-химические свойства смеси
Исполнение пробоотборника
Общая геометрия пробоотборника может повлиять на отбираемый образец. Производители фармацевтической продукции используют либо пробоотборники, доступные в коммерческой сети, либо изготовляют собственные пробоотборники. Пробоотборники обычного исполнения состоят из двух концентрических тубусов. Внутренний тубус цельный, с одной или двумя камерами, которые позволяют набирать пробу. Наружный тубус полый, в нем имеются отверстия, которые установлены против камер во внутреннем тубусе. Правильное исполнение характеризуется острым наконечником, который облегчает попадание в нерасфасованную порошковую массу. Рукоятка, расположенная на верхнем конце, используется для поворота внутреннего тубуса таким образом, чтобы пробоотборник открывался или закрывался. В идеальном случае в ходе пробоотбора закрытый пробоотборник погружается внутрь порошкового слоя в нужном месте. После чего пробоотборник открывается и, тем самым, создается возможность попадания пробы материала в камеру (либо в камеры) внутреннего тубуса. Наконец пробоотборник закрывается, вытягивается из массы, проба высыпается, собирается и подвергается анализу
Имеются в наличии проботборники различной длины и размера (разное число, размер и геометрия пробоотборных камер). Некоторые пробоотборники имеют множество камер, которые находятся в его боковой части. Такой тип пробоотборника можно использовать для отбора множественных образцов с разной глубины внутри слоя или отдельной пробы с четко определенного места.
Методика пробоотбора
Методика пробоотбора - второй фактор, который может повлиять на ошибку в пробоотборе. При погружении пробоотборника в слой порошка слой деформируется за счет того, что материал из верхних слоев вносится вниз по направлению к низшим слоям. Теоретически размер такой деформации может зависеть от того, как пробоотборник погружается в слой - мягким, резким или вращающимся движением. Угол, под которым пробоотборник погружается в слой порошка, может повлиять на ошибку пробоотбора (например, было доказано, что пробоотборник, погружаемый в перпендикулярном направлении, может вынести образцы с частицами, размер которых отличается от ситуации, когда тот же пробоотборник погружается в слой под острым углом). Кроме того, на пробоотборнике, который погружается под острым углом, камера пробоотбора может быть повернута в ходе пробоотбора о направлению вниз (6:00) либо вверх (12:00), либо где-то между этими точками. То есть, важно, чтобы оператор получал образцы одним и тем же методом.
Ошибка пробоотбора может также зависеть от глубины слоя, поскольку статическое давление нерасфасованного слоя порошка вдавливает материал в камеру пробоотбора. Это давление значительно выше на дне большого контейнера, чем посредине или близко к поверхности.
Физико-химические свойства смеси
Силу, необходимая для погружения длинного пробоотборника в толстый слой порошка, также следует предвидеть. Эта сила зависит от физических свойств состава смеси и может привести к утрамбовке смеси, истиранию различных частиц и другим деформациям слоя. Если смесь характеризуется широким диапазоном распространения по размеру частиц, то может произойти проникновение мелкого материала в грубый материал, за счет чего получаются образцы, которые не будут репрезентативными для нерасфасованной смеси.
Кроме того, если пробоотборник используется для отбора проб из гомогенной смеси, которая состоит из порошков с различными характеристиками текучести, то порошок с медленной текучестью будет в первую очередь набираться в камеры пробоотборника, что в результате также приведет к наличию нерепрезентативного образца.
Некоторые API и вспомогательные вещества могут также прилипать к поверхности пробоотборника, что может привести к измеряемой ошибке пробоотбора, особенно для продуктов с низкой концентрацией лекарственного средства.
Эффективность пробоотборника была лучше всего обобщена Теренсом Алланом в его монографии об измерении частиц:
"Правильность или неправильность пробоотборной иглы сравнима с правильностью отбора проб с помощью совка и в целом от ее использования следует отказаться."
К сожалению, заключение судьи Уолина заставило производителей фармацевтической продукции заниматься этой неадекватной технологией в ходе валидации процесса и в ходе рутинного производства. Поэтому сотрудниками исследовательских лабораторий следует перед собственно валидацией процесса дать оценку описанных выше факторов и их влияния на однородность для каждого состава продукта.
Количество пробы
Перед собственно валидацией следует также определить минимальное количество пробы, которое будет адекватно распространению активного вещества для данного состава смеси и для данного производственного процесса. Как правило, такие исследования проводятся в ходе разработки продукта и включают:
· контроль за альтернативами по количеству пробы смеси как кратного массы таблетки или капсулы (например, 1х, Зх, 5х, 10х 20х, 30х и т.д.)
· для каждого количества пробы следует брать несколько образцов смеси из нескольких точек (не меньше 10)
· каждый образец смеси анализируется как целое без дальнейшего деления
· для каждого количества образца смеси рассчитывается среднее значение и стандартное отклонение образца
· проводится пробоотбор продукта (таблеток или капсул), анализ и расчет среднего значения и стандартного отклонения
· выполняется Т-тест для сравнения средних значений содержания в смеси и в продукте
· выполняется F-тест для сравнения стандартных отклонений содержания в смеси и в продукте
· оценка результатов выполняется по таблице
| Статистическая классификация смесей и продуктов |
||
| Результат | Статистические заключения | Замечания |
| А | SD смеси
|
Склонность к неравномерности образца не отмечена. Такой результат считается удовлетворительным. Минимальное количество образца, для которого действуют такие условия, следует использовать для валидации однородности смеси |
| В |
SD смеси > SD продукта
|
Индицирует склонность к неравномерности. Между ф существует значительная разница, которая индицирует факт, что пробы не были взяты из одного и того же комплекса. SDCMeCH >SDnp0flyKTa, что доказывает неравномерность пробоотбора |
| С |
SD смеси
|
Индицирует склонность к неравномерности. Между ф существует значительная разница, которая индицирует факт, что пробы не были взяты из одного и того же комплекса. |
| D |
SD смеси > SD продукта
|
Происходит либо большая неравномерность по образцам (методика отбора проб), либо происходит значимое перемешивание. Можно решить с помощью анализа рассеяния |
В идеальном случае (когда нет проблем с пробоотбором из смеси) для каждого количества пробы стандартное отклонение образца смеси не больше^ чем у продукта, а средние значения образцов смеси и продукта не показывают значимой разницы (результат А). В таком случае рекомендуется минимальный практический образец.
Если же для образцов меньшего размера будут получены результаты В или С, а для образца большего размера будет получен результат А, который держится и для еще большего количества, то подходящее количество образца соответствует тому количеству, в котором как в первом был отмечен результат А.
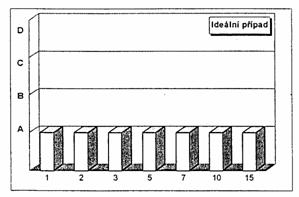
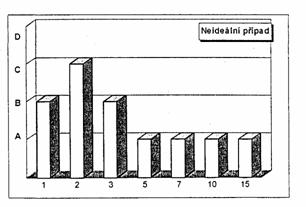
Если обнаруживается результат D для всех количеств, то следует рассмотреть склонность к неравномерности образца с помощью анализа рассеяния компонент.
Оптимизация параметров процесса
Перед собственно демонстрацией эффективности процесса перемешивания порошковых смесей следует также проверить важнейшие параметры процесса, т.е. способ, скорость и время перемешивания.
Способ перемешивания обычно обусловлен техническими возможностями доступных установок. Перед собственно валидацией он должен быть в достаточной степени описан.
Скорость перемешивания также ограничена техническим исполнением установки. В случае, если скорость перемешивания устанавливается, необходимо в рамках оптимизации процесса выбрать наиболее приемлемую скорость для получения гомогенной смеси с подходящими физико-химическими параметрами.
Время перемешивания должно демонстрироваться для каждого процесса перемешивания (часто эта операция включается в валидацию). Если параметры способа и скорости перемешивания четко установлены, можно демонстрировать время перемешивания следующим образом:
· в соответствии с геометрией смесителя (гомогенизатора) предлагается число точек пробоотбора, порядок отбора и количество пробы
· с учетом предполагаемого времени перемешивания предлагается 5-10 интервалов для отбора проб из каждой точки
· в ходе приготовления смеси проводится пробоотбор по описанному выше плану, образцы анализируются с помощью соответствующих методов
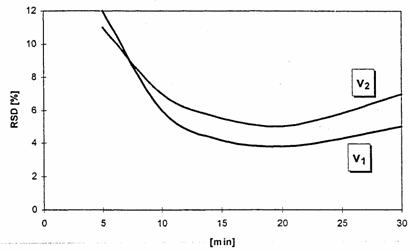
· из полученных результатов строится график зависимости RSD индивидуальных образцов от времени
· рекомендованное время перемешивания должно выдержать критерий для RSD смеси, как будет описано ниже
· в случае, если обнаружится ошибка пробоотбора, следует приведенный способ расширить в соответствии с требованиями за счет анализа рассеяния компонент либо использовать в качестве критерия приемлемости минимальное значение RSD
Приведенный способ имеет ряд недостатков. В первую очередь это высокие технические требования к конструкции точек пробоотбора. В случае, если смеситель не оснащен пробоотборником, приходится прерывать процесс перемешивания (неадекватный процесс). Кроме того, в результате такого способа получается смесь продукта, которая обычно характеризуется неподходящей вариабельностью API (влияние сегрегации), так что бывает сложно такие продукты отпустить на реализацию. Поэтому иногда для подобных исследований используется плацебо, которое с другой стороны не отражает с точностью свойства продукта.
Голистический подход к валидации однородности смеси
В связи с тем, что надежда на выпуск удовлетворительного продукта при несовершенном перемешивании очень невелика, совершенный контроль финишного продукта может предоставить ценную информацию об операции перемешивания. Какой смысл в получении гомогенной порошковой смеси, если последующая сегрегация частиц даст продукт, который не соответствует спецификации. Правильная оценка продукта поможет установить определенные заключения о возможном появлении ошибки при пробоотборе из смеси.
PDA предложила так называемую концепцию "голистического подхода" для валидации однородности смеси (см. таблица), которая предполагает, что общий прогноз эффективности перемешивания и диапазон последующей сегрегации частиц после смешивания можно получить за счет тщательной оценки смеси и продукта. Только в случае, когда принимаются во внимание совместно оба состояния (т.е. смесь и продукт), можно получить правильную оценку операции перемешивания. Если же кроме этого будет подтверждена ошибка пробоотбора, PDA рекомендует использовать альтернативный анализ, который позволит откорректировать источник такой ошибки.
| ГОЛИСТИЧЕСКИЙ ПОДХОД |
||
| Шаг |
Процедура |
Замечания |
| 1 |
Оценка однородности продукта |
Используются адекватные критерии приемлемости (метод Бергема, предельные допуски) |
| 2 |
Оценка однородности смеси |
Используются адекватные критерии приемлемости (SDPI, метод Бергема, предельные допуски и т.п.) |
| 3 |
Определение статуса валидации |
а) если продукт и смесь выдерживают соответствующие критерии приемлемости, валидация считается успешной |
| б) если продукт не выдерживает критерии приемлемости, ваидация не считается успешной |
||
| В) если продукт выдерживает критерии приемлемости, но смесь не выдерживает критерии приемлемости, то следует расширить валидацию (например, виляние ошибки пробоотбора) |
||
| 44 |
Статистическая классификация смеси и продукта |
а) если будет обнаружено условие А, ошибка пробоотбора не индицируется |
| б) если будет обнаружено условие В, С или D, то возможна индикация ошибки пробоотбора |
||
| 55 |
Анализ рассеяния компонент |
Анализ рассеяния компонент предоставляет еще одно подтверждение наличия факта ошибки пробоотбора. Кроме того, если однородность смеси приемлемая, он позволит провести и другую оценку |
Шаг 1: Оценка однородности продукта
Для проверки однородности продукта обычно используется фармакопейный многоступенчатый тест. Поскольку требования в USP, Eur.Pharm., HL (Чешская фармакопея) практически тождественны (см. таблицы), ниже по тексту будут приведены только требования USR
В USP, кроме того, еще приводится требование к RSD, которое должно быть для 1-й ступени теста < 6 %, а для 2-й ступени теста < 7,8 %.
| Таблетки |
||||
| Ступень/ число образцов |
Число единиц в пределах |
Результат |
||
| 85-115% |
75- 125% (за пределами 85-1 15) |
за пределами 75-125% |
||
| 1-я ступень/ 10 |
10 |
0 |
0 |
ОК |
| 9 |
1 |
0 |
2-я |
|
| <9 |
> 1 |
0 |
NOK |
|
| <10 |
>0 |
NOK |
||
| 2-я ступе нь/+20 |
29 |
1 |
0 |
ОК |
| <29 |
> 1 |
0 |
NOK |
|
| <30 |
- |
>0 |
NOK |
|
| Капсулы |
||||
| Ступень/ число образцов |
Число единиц в пределах |
Результат |
||
| 85-115% |
75- 125% (за пределами 85-1 15) |
за пределами 75-125% |
||
| 1-я ступень/ 10 |
19 |
0; 1 |
0 |
ОК |
| <9 |
2;3 |
0 |
2-я |
|
| <7 |
>3 |
0 |
NOK |
|
| <10 |
>0 |
_НО1С |
||
| 2-я ступень/+20 |
27; 28 |
2;3 |
0 |
ОК |
| <27 |
>3 |
0 |
NOK |
|
| <30 |
- |
>0 |
NOK |
|
Однако, для определения приемлемой однородности продукта используются в рамках валидации более строгие методы, как, например:
· метод Бергема
· предельные допуски
Метод Бергема- отличный инструмент для доказательства способности серии таблеток или капсул соответствовать требованиям по однородности состава. Этот метод сначала требует определения вероятности (обычно 95%) во исполнение требований теста на однородность состава по USP.
Затем необходимо выделить совместную область надежности стандартного отклонения и среднего арифметического значения образцов (так называемую, характеристическую кривую). Это обеспечивает для специфицированного уровня надежности (обычно 90%), что образец был взят из комплекса в рамках этой области и с 95% вероятностью он будет удовлетворять требованиям теста на однородность по USP.
В таблицах приводятся значения вариационных коэффициентов (или RSD) для данного средне арифметического значения (выраженного в % от декларированного значения) и данное число образцов. Вариационный коэффициент образца меньший или равный критическому вариационному коэффициенту предоставляет 90% уверенность в том, что не меньше 95% всех образцов, которые были тестированы на однородность, выдерживают требования к тесту по USP для таблеток или капсул.
Критические значения RSD (Бергем) для удовлетворения требований теста USP на однородность содержания (состава) таблеток
| Число образцов |
Средний уровень содержания (% заявленного значения) |
||||
| 90 |
95 |
100 |
105 |
110 |
|
| 10 |
1,18 |
2,23 |
3,17 |
2,02 |
0,96 |
| 20 |
1,50 |
2,85 |
4,01 |
2,58 |
1,23 |
| 30 |
1,66 |
3,15 |
4,39 |
2,85 |
1,35 |
| 40 |
1,76 |
3,33 |
4,61 |
3,01 |
1,44 |
| 50 |
1,83 |
3,45 |
4,75 |
3,12 |
1,49 |
| 60 |
1,88 |
3,55 |
4,86 |
3,21 |
1,54 |
| 70 |
1,92 |
3,63 |
4,94 |
3,29 |
1,56 |
| 100 |
2,00 |
3,78 |
.5,11 |
3,42 |
1,64 |
Обратите внимание, что величине числа образцов 10 и при 100 % среднем декларированном значении требуется, чтобы RSD для таблеток было < 3,17 критическое значение). Если число образцов вырастет до 30, требуется значение RSD < 4,39 (критическое значение). Такие требования значительно превышают по строгости и собственно тест по USP.
Критические значения RSD (Бергем) для удовлетворения требований теста USP на однородность содержания (состава) капсулок
| Число образцов |
Средний уровень содержания (% заявленного значения) |
||||
| 90 |
95 |
100 |
105 |
110 |
|
| 10 |
1,48 |
2,79 |
3,67 |
2,52 |
1,21 |
| 20 |
1,92 |
3,63 |
4,51 |
3,29 |
1,57 |
| 30 |
2,13 |
4,03 |
4,87 |
3,65 |
1,75 |
| 40 |
2,27 |
4,28 |
5,08 |
3,88 |
1,85 |
| 50 |
2,37 |
4,46 |
5,22 |
4,04 |
1,94 |
| 60 |
2,44 |
4,59 |
5,32 |
4,16 |
2,00 |
| 70 |
2,50 |
4,69 |
5,41 |
4,26 |
2,05 |
| 100 |
2,61 |
4,91 |
5,57 |
4,46 |
2,14 |
Шаг 2: Оценка однородности смеси
Мерой однородности смеси считается стандартное отклонение активного вещества в смеси, поскольку оно не зависит от систематической ошибки пробоотбора.
Для оценки однородности смеси в рамках валидации используются следующие методы:
• предполагаемый интервал стандартного отклонения (SDPI)
• метод Бергема (когда среднее арифметическое значение смеси значимо отличается от действительного содержания, этот метод ненадежен)
• предельные допуски (см. метод Бергема, ограниченный диапазон)
• отдельные образцы и RSD (рекомендует FDA)
- все образцы должны находиться между 90 - 110 % декларированного значения
- RSD должны быть меньше, чем 5 %
- число образцов должно быть не меньше 10
• индекс возможностей
Наиболее распространенный метод - это метод доверительного интервала стандартного отклонения (SDPI), который дает возможность предвидеть у образца величины п со специфицированным уровнем достоверности диапазон стандартного отклонения будущего образца величиной m из того же множества. Для наших целей будем рассматривать только верхний предел стандартного отклонения будущего образца, так что будем использовать интервал только с одной стороны.
SDPI можно легко рассчитать с помощью таблиц F-значений. Специфически для данного теста величина числа будущего образца 10 (для 1-й ступени теста по USP). Критическое стандартное отклонение для образца смеси, которое гарантирует, что будущий образец будет удовлетворять требованиям теста USP, рассчитывается следующим образом:
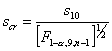
где n = величина обычного образца
scr = критическое стандартное отклонение
s10 = верхний предел будущего образца величиной 10
1 - a = доверительный интервал (напр. 0,9)
F = табличное значение F по тесту Фишера
Можно вывести, что 6% стандартное отклонение целевой концентрации множества предоставляет высокую степень вероятности (95,7 %), что смесь пройдет тест USP для таблеток, если множество центрировано на целевые 100%. Поэтому рекомендуется, чтобы верхний предел стандартного отклонения, был выражен зависимостью:
s10 = 0,06 х [ целевая концентрация ]
SDPI дает возможность рассчитать максимальное (т.е. критическое) приемлемое стандартное отклонение для образцов с п единичными дозами финишной смеси, которые отбирают в ходе валидации (см. таблица).
Если будет рассчитано стандартное отклонение образца Sn< Scr' то гаРантиРУется с минимальной достоверностью 100 (1 - а)%, что верхний упреждающий предел стандартного отклонения будущего образца с величиной числа 10 будет < 6% от целевой концентрации и удовлетворит требованиям теста на однородность содержания API в готовой продукции по USP.
| Предельное стандартное отклонение (90% доверительный интервал), которое гарантирует, что 10 будущих единиц будет иметь RSD < 6% |
|||||||
| N - |
scrr |
N |
scr |
N |
Scr |
N |
scr |
| 10 |
3,841 |
30 |
4,403 |
50 |
4,519 |
70 |
4,570 |
| 11 |
3,916 |
31 |
4,413 |
51 |
4,523 |
71 |
4,572 |
| 12 |
3,979 |
32 |
4,421 |
52 |
4,526 |
72 |
4,573 |
| 13 |
4,033 |
33 |
4,429 |
53 |
4,529 |
73 |
4,575 |
| 14 |
4,079 |
34 |
4,437 |
54 |
4,532 |
74 |
4,577 |
| 15 |
4,119 |
35 |
4,445 |
55 |
4,535 |
75 |
4,578 |
| 16 |
4,154 |
36 |
4,451 |
56 |
4,538 |
76 |
4,580 |
| 17 |
4,185 |
37 |
4,458 |
57 |
4,541 |
77 |
4,581 |
| 18 |
4,213 |
38 |
4,464 |
58 |
4,544 |
78 |
4,583 |
| 19 |
4,238 |
39 |
4,470 |
59 |
4,546 |
79 |
4,584 |
| 20 |
4,260 |
40 |
4,476 |
60 |
4,549 |
80 |
4,586 |
| 21 |
4,280 |
41 |
4,481 |
61 |
4,551 |
81 |
4,587 |
| 22 |
4,299 |
42 |
4,486 |
62 |
4,554 |
82 |
4,588 |
| 23 |
4,316 |
43 |
4,491 |
63 |
4,556 |
83 |
4,590 |
| 24 |
4,331 |
44 |
4,496 |
64 |
4,558 |
84 |
4,591 |
| 25 |
4,346 |
45 |
4,500 |
65 |
4,560 |
85 |
4,592 |
| 26 |
4,359 |
46 |
4,504 |
66 |
4,562 |
86 |
4,593 |
| 27 |
4,371 |
47 |
4,508 |
67 : |
4,564 |
87 |
4,595 |
| 28 |
4,383 |
48 |
4,512 |
68 |
4,566 |
88 |
4,596 |
| 29 |
4,393 |
49 |
4,516 |
69 |
4,568 |
89 |
4,597 |
Шаг 3: Определение статуса валидации
Если продукт и смесь выдерживают по отдельности свои критерии приемлемости, валидация считается успешной. Если же продукт не выдерживает критерии приемлемости, то валидация не считается успешной, невзирая на результаты испытаний смеси. Если же продукт выдерживает критерии приемлемости, а смесь не выдерживает их, то следует выполнить дальнейшее расследование. Причиной может быть, например, ошибка пробоотбора. Перед тем, как продолжить валидацию в таком случае следует руководствоваться методами для результатов вне рамок (за пределами) спецификации.
Шаг 4: Статистическая классификация смеси и продукта
Методы классификации для среднего арифметического и стандартного отклонения уже были описаны (см. тезисы о численности пробы - образца). Если предполагаестя занчимая ошибка пробоотбора смеси, то можно воспользоваться специальным (гнездовым) планом отбора пробы смеси и продукта и продолжать методом анализа рассеяния компонент (шаг 5).
Шаг 5: Анализ рассеяния/синтезом
Применяется в случае, если продукт удовлетворительно прошел строгий статистический тест на однородность (например, метод Бергема), но ошибка при пробоотборе вероятно вызвала, что смесь не выдержала требуемый критерий (SDPI). В таком случае можно воспользоваться методом, опирающемся-наанализ рассеяния компонент, который в статистике описан как анализ рассеяния - модель случайных влияний (факторов). Сила этого статистического инструмента заключается в сепарации общей изменчивости в частные компоненты.
Анализ рассеяния смеси
При приложении анализа рассеяния к процедуре перемешивания можно считать, что в общей изменчивости содержания API в смеси (обусловленной рассеянием ас2) участвует как "макро" компонент (между разными точками; рассеяние ад2), так и "микро" компонент (в рамках одной точки; рассеяние ав2). При условии, что процессы, вызывающие оба рассеяния, взаимно независимы, действует:
![]()
Исходя из этого уравнения, можно с помощью статистических расчетов выполнить прогнозирование обеих частных компонент.
Компонента между разными точками (макро - компонент) в смеси представляет собой рассеяние, которое связано с макроизменениями в среде смеси. Это компонента, которая отражает общую однородность смеси и который служит для прогнозирования минимального времени получения удовлетворительной смеси. Эта компонента зависит по меньшей мере от следующих факторов:
• распределение API в макро масштабе (рассеяние ![]()
• точность аналитического теста (рассеяние ![]() )
)
Если вновь предположить взаимонезависимость процессов и пренебречь остальными факторами, то получим зависимость:
![]()
Теоретически можно предугадать оба приведенных фактора, которые виляют на макро - компоненту общего рассеяния, но на практике для такого прогнозирования понадобится большое количество результатов, по этой причине подобный анализ выполняется только в очень редких случаях (то же самое будет действовать и для остальных макро и микро компонент). Мы приводим такие зависимости только по причине объяснения зависимости отдельных компонент от индивидуальных процессов.
Компонента в рамках точки (микро - компонента) в смеси - это рассеяние, на которое больше всего влияет ошибка пробоотбора. Эта компонента зависит по меньшей мере от следующих факторов:
• ошибка пробоотбора (рассеяние ![]() )
)
• распределение АР1в микро масштабе (рассеяние ![]() )
)
• точность аналитического теста (рассеяние ![]() )
)
Если опять предположить взаимонезависимость процессов и пренебречь остальными факторами, то получим зависимость:
![]()
Для прогнозирования обеих компонент (т.е. рассеяний ад2, ав2) используется специальный план пробоотбора. В зависимости от геометрии смесителя (гомогенизатора) или контейнера сначала выбирают 4-10 точек, которые должны включать и вероятные мертвые точки. Из каждой точки отбирают 3-6 образцов (всегда одинаково).
На следующем рисунке приведен пример для 1 0 точек, из которых отбирались по 3, т.е. всего было взято 30 проб.
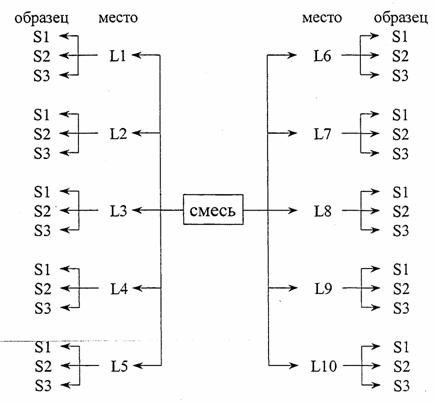
По результатам анализов этих 30 образцов смеси были рассчитаны следующие статистические параметры:
| Статистика |
Ст.свободы |
Критическое RSD |
Результат |
| Рассеяние между точками 1,797 |
|||
| Рассеяние в пределах точки 25,11 |
20 |
||
| Общее 26.907 |
(1) |
SDPI |
|
| RSD 5,187 |
4,403 |
NOK |
Как видно из таблицы, расчетное значение RSD = 5,187 больше, чем критическое значение 4,403 для метода SDPI. То есть, однородность содержания API в смеси не выдержала критерии приемлемости метода SDPI.
При более подробном анализе результатов также видно, что в общем рассеянии (26,907) больший удельный вес рассеяния в пределах одной точки (25,11), что может быть вызвано ошибкой пробоотбора.
Анализ рассеяния продукта
Подобный метод можно использовать и для стадии приготовления продукта (например, таблеток). При прессовании периодически отбирают образцы таблеток всегда по одной из каждой позиции на таблетпрессе (всего 10-100). Для простоты рассматриваем эти образцы как образцы из „одной чашки". В ходе прессования таблеток одной серии отбирают всего 6-12 „чашек". Из каждой чашки потом случайно отбирают индивидуально 3-6 таблеток, в которых определяется содержание API.
Общая изменчивость содержания API в таблетках (дана рассеянием ![]() ) опять состоит из двух компонент. Первая - это рассеяние между чашками (
) опять состоит из двух компонент. Первая - это рассеяние между чашками (![]() ), вторая - рассеяние в пределах одной чашки (
), вторая - рассеяние в пределах одной чашки (![]() ). При условии взаимной независимости макро и микро процессов действует:
). При условии взаимной независимости макро и микро процессов действует:
![]()
Компонента между чашками представляет рассеяние поперек серии, иначе говоря, рассеяние между отдельными чашками. Эта компонента зависит по меньшей мере от следующих факторов:
• распределение API в макро масштабе (рассеяние ![]()
• точность аналитического теста (рассеяние ![]() )
)
При условии взаимной независимости процессов и пренебрежении остальными факторами действует:
![]()
Компонента в пределах одной чашки включает все источники изменчивости, кроме источника между отдельными точками. Эта компонента зависит по меньшей мере от следующих факторов:
• распределение API в микро масштабе (рассеяние ![]() )
)
• точность аналитического теста (рассеяние ![]() )
)
При условии взаимной независимости процессов и пренебрежении остальными факторами действует:
![]()
Из сравнения данных уравнений с подобными уравнениями для анализа рассеяния смеси вытекает, что рассеяние ![]() не включает ошибку пробоотбора, в то время, как рассеяние
не включает ошибку пробоотбора, в то время, как рассеяние ![]() эту ошибку включает. Поскольку остальные составляющие в обоих рассеяниях практически идентичны, наличие значимого неравенства между обоими рассеяниями (
эту ошибку включает. Поскольку остальные составляющие в обоих рассеяниях практически идентичны, наличие значимого неравенства между обоими рассеяниями (![]() ) будет, вероятно, вызвано ошибкой пробоотбора.
) будет, вероятно, вызвано ошибкой пробоотбора.
В следующем примере будет с помощью анализа рассеяния проведена оценка продукта (таблетки), который был изготовлен из описанной выше "неудовлетворительной" смеси. В ходе процесса таблетирования было отобрано всего 5 чашек, а из каждой чашки отбирали всегда по 10 таблеток, т.е. в общей сложности 50 образцов. Из результатов анализов были рассчитаны следующие статистические параметры:
| Статистика |
Ст.свободы |
Критическое RSD |
Результат |
||||
| Рассеяние между чашками 0,39 |
45 (0 |
||||||
| Рассеяние в рамках 1 чашки 1,034 |
|||||||
| Общее 424 |
Bergum |
||||||
| RSD 1,193 |
4,75 |
ОК |
Из таблицы видно, что продукт выдержал жесткие критерии метода Бергема. При сравнении с результатами по смеси очевидна значительная разница по результатам рассеяния в пределах точки пробоотбора и в пределах одной чашки.
Полученные результаты показали, что несмотря на то, что смесь не удовлетворяет критериям по однородности, продукт был однородным. Результаты приведенного примера можно изобразить графически следующим образом:
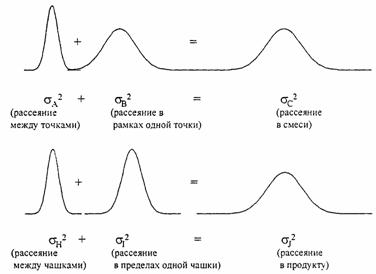
Вероятность того, что из "неудовлетворительной" смеси можно получить "удовлетворительный" продукт без специальной процедуры, весьма незначима. Поэтому можно предположить, что результаты, которые привели к отрицательному заключению по смеси, не были получены на образцах, которые представляли смесь в полном разрезе.
Статистические тесты по стандартному отклонению и средним значениям смеси и продукта далее показали, что классификация продукта проводилась в условиях D. Причиной неудовлетворительного результата по смеси была, вероятно, ошибка пробоотбора (рассеяние смеси в пределах точки пробоотбора-имеет максимальный удельный вес в общем рассеянии смеси).
Анализы с помощью синтеза
Для исключения ошибки пробоотбора PDA ввела так называемое общее эффективное рассеяние смеси (![]() ), которое получают из суммы рассеяния компоненты точки из смеси (
), которое получают из суммы рассеяния компоненты точки из смеси (![]() ) и рассеяния компоненты продукта из одной "чашки" (
) и рассеяния компоненты продукта из одной "чашки" (![]() ):
):
![]()
В этой связи, эффективное рассеяние будет содержать макро -компоненту для смешивания между точками смеси и микро - компоненту в пределах одной точки (чашки). Таким путем получаем статистический прогноз общего эффективного рассеяния с исключением влияния нерепрезентативного пробоотбора. Если такое общее эффективное рассеяние смеси выдерживает критерии приемлемости (метод SDPI), однородность смеси считается удовлетворительной.
„Такой метод PDA называет анализом с помощью синтеза."
Использование анализа рассеяния для описанного выше примера приводит к расчету общего эффективного рассеяния 1,797 + 1,034 = 2,831, что соответствует RSD = 1,683.
Для прогноза критического значения RSD по методу SDPI необходимо, однако, определить адекватную ступень свободы. Последнюю, как правило, определяют с помощью аппроксимации Саттертуэйта. В некоторых случаях в результате получается число, меньшее, чем любая из ступеней свободы, связанная с отдельными квадратами степеней свободы, которые используются для данного расчета. В таких случаях предлагается использовать степень свободы, которая будет не меньше, чем минимальная из названных квадратов степеней свободы. Поэтому была выбрана степень свободы 9 как адекватная степень для общего рассеяния синтеза (т.е., число образцов для анализа синтезом N = 10). Такой степени отвечает критический коэффициент изменчивости (или RSD) 3,841.
Из сравнения эффективного RSD = 1,683 (рассчитанного из общего эффективного рассеяния) с критическим значением 3,841 вытекает, что анализ синтезом подтверждает удовлетворительную однородность "эффективной" смеси..
Такой подход позволяет выполнять оценку однородности смеси без наличия значимой ошибки пробоотбора смеси.
| Статистика |
Ст.свободы |
Критическое RSD |
Результат |
| Рассеяние между точками 1,797 |
|||
| Рассеяние в пределах одной L 1,034 |
45 |
||
| Общее 2,831 |
9(1) |
SDPI |
|
| RSD 1,683 |
3,841 |
ОК |
Аналитический метод
Для оценки однородности смеси или продукта следует использовать только отвалидированные аналитические методы. PDA отдает предпочтение методу HPLC, для которого необходимо во всех случаях взвесить или решить следующие аспекты:
• визуальный контроль образцов (внешний вид смеси, деформация таблеток, и т.п.)
• тестирование образца целиком без деления (т.е., количественный перевод образца в растворитель либо в мобильную фазу)
• определение массы образцов смеси
• спаривание приготовления образцов
• определение содержания в смеси либо в финишном продукте (спаренные набрызги, определение точности)
• анализы стандартов в определенных интервалах (спаренные набрызги, определение точности)
• результаты анализов в массовых % либо и в % заявленного содержания
• документированные параметры для оценки пиков (разрешающая способность, высота теоретических этажей, симметрия, и т.п.)
Оценка результатов вне пределов спецификации (OOS)
Удовлетворительное объяснение результатов по смеси, которые вышли за рамки пределов спецификации, -критический фактор решения проблематики однородности смеси в ходе валидации процесса. Оценка должна опираться на адекватное расследование, которое, в свою очередь, адекватно документировано и утверждено QA/QC.
1-я фаза: Предварительное лабораторное расследование может
быть полезным для определения, если результаты OOS получаются за счет неправильного обращения с образцом или за счет неправильного лабораторного тестирования (ошибка аналитического метода, стандарта, исполнения на приборах, и т.д.). Ошибки следует рассматривать с позиции их возможных последствий на результаты тестов остальных образцов. Недопустимо признать недействительным только один результат вне пределов спецификации - OOS, если от него зависят и остальные результаты.
2-я фаза: Если в ходе предварительного лабораторного расследования не будут найдена причина результатов OOS, следует расширить расследование. Расследование следует направить на то, был ли надлежащим образом выполнен пробоотбор и обращение с образцом, а также, появились ли нетипичные проблемы производственного процесса (отклонения исходных материалов, полупродукта, оборудования, процессов, параметров процесса или среды).
Все отклонения должны быть расследованы на значимость и возможные последствия на результаты OOS. Если результат OOS вызван недопустимым отклонением процесса, такую серию следует исключить из валидационного тестирования.
3-я фаза: Если для результата OOS не будет найдена обоснованная лабораторная ошибка или ошибка производственного процесса, следует расширить расследование за счет оценки возможной ошибки пробоотбора. Следует использовать методы:
• оценки результатов тестов на однородность смеси
• оценки однородности содержания продукта
• сравнения результатов однородности содержания продукта с результатами по смеси с применением методов статистического анализа (F-тест, Т-тест, метод сравнения рассеяния, и т.д.)
Заключение
Процесс смешивания - единичная операция, которая требует специфической валидации. Комиссия PDA считает рекомендации, касающиеся количества образца и критериев приемлемости, которые приведены в решении судьи Уолина, необоснованными с учетом правильности и воспроизводимости современной технологии пробоотбора. Поскольку следующие шаги процесса часто влияют на однородность смеси, следует уделять внимание оценке валидации в целом и оценке общей приемлемости однородности смеси. Этот процесс включает также оценку результатов по однородности содержания в готовой продукции и сравнение соответствия этих результатов с результатами по смеси.
Из последних проектов FDA по дополнению правил современного GMP очевидно, что следует выполнять тестирование на однородность содержания активного вещества в финишной смеси при рутинном производстве, невзирая на адекватную валидацию процесса и другие виды контроля, наличия которых требует GMP.

